Page 122 - kpiebook65064
P. 122
72 โครงการสังเคราะห์ข้อเสนอ
เพื่อเสริมสร้างการอภิบาลระบบยา
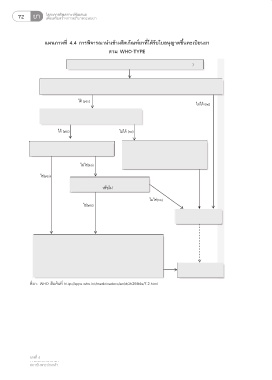
แผนภาพที่ 4.4 การพิจารณานำเข้าผลิตภัณฑ์ยาที่ได้รับใบอนุญาตขึ้นทะเบียนยา
ตาม WHO-TYPE
แผนภาพที่ 4.4 การพิจารณาน าเข้าผลิตภัณฑ์ยาที่ได้รับใบอนุญาตขึ้นทะเบียนยาตาม WHO-TYPE ข้อคิดเห็น[N4]: format รูปพัง ต้องท าใหม่
ข้อคิดเห็น[N5]: ต้องอธิบายกระบวนการ 1
ได้รับใบรับรองชนิดของผลิตภัณฑ์จาก WHO (Obtain WHO-Type product )
2 3 4 ว่ามันท าอย่างไร เพราะดูจากลูกศร
แล้วสับสน
สามารถเชื่อถือการรับรองของประเทศผู้ส่งออกได้หรือไม่
(Do you intend to rely on exporting country's authority?)
ได้ (yes) ไม่ได้ (no)
ผลิตภัณฑ์ได้รับสิทธิในการจัดจ าหน่ายในประเทศผู้ส่งออกหรือไม่
(Does product has marketing authorization in exporting country?)
ได้ (yes) ไม่ได้ (no)
เป็นผลิตภัณฑ์ที่เหมือนกับในประเทศผู้ส่งออกหรือไม่ พิจารณาเหตุผลที่ผลิตภัณฑ์นั้นไม่ได้สิทธิการจัด
(Is the product the same as in exporting country?)
จ าหน่ายในประเทศผู้ส่งออก
ไม่ใช่(no) (Consider whether there is reasonable justification for
the product to originate from the exporting country)
ใช่(yes)
ความแตกต่างของผลิตภัณฑ์นั้นเป็นที่ยอมรับ
หรือไม่
หรือไม่
ไม่ใช่(no)
ใช่(yes)
ประเมินผล
(Make your own assessment)
- ตรวจสอบผลิตภัณฑ์ขั้นสุดท้ายในห้องทดลอง
(Check whether analytical methods for finishedproduct can be applied at national QC
lab)
- ทบทวนข้อมูลผลิตภัณฑ์และข้อความบนฉลาก
(Review, and, if necessary, adapt, product information and labeling)
ประกาศผลการประเมิน
- ประเมินความสามารถในการออกฤทธิ์ (Assess interchangeability, if required)
(Issue decision )
ที่มา: WHO สืบค้นที่ http://apps.who.int/medicinedocs/en/d/Jh2994e/7.2.html
ที่มา: WHO สืบค้นที่ http://apps.who.int/medicinedocs/en/d/Jh2994e/7.2.html
4-9
บทที่ 4
สถาบันพระปกเกล้า