Page 181 - kpiebook65064
P. 181
โครงการสังเคราะห์ข้อเสนอ 131
เพื่อเสริมสร้างการอภิบาลระบบยา
แผนภาพที่ 5.10 ขั้นตอนการขึ้นทะเบียนต ารับยาสามัญใหม่ (New Generic Drugs)
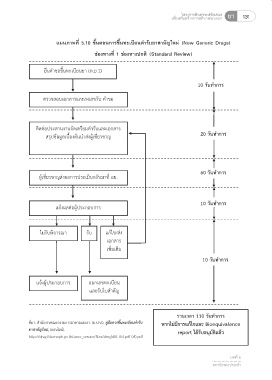
แผนภาพที่ 5.10 ขั้นตอนการขึ้นทะเบียนตำรับยาสามัญใหม่ (New Generic Drugs)
ช่องทางที่ 1ช่องทางปกติ (Standard Review)
ช่องทางที่ 1 ช่องทางปกติ (Standard Review)
ยื่นค าขอขึ้นทะเบียนยา (ท.ย.1)
10 วันท าการ
ตรวจสอบเอกสารและลงเลขรับ ค าขอ
ติดต่อประสานงานจัดเตรียมต ารับและเอกสาร
สรุปข้อมูลเบื้องต้นน าส่งผู้เชี่ยวชาญ 20 วันท าการ
60 วันท าการ
ผู้เชี่ยวชาญส่งผลการประเมินกลับมาที่ อย.
10 วันท าการ
แจ้งผลต่อผู้ประกอบการ
ไม่รับพิจารณา รับ แก้ไข/ส่ง
เอกสาร
เพิ่มเติม
10 วันท าการ
แจ้งผู้ประกอบการ ออกเลขทะเบียน
และรับใบส าคัญ
รวมเวลา 110 วันท าการ
ที่มา: ส านักงานคณะกรรมการอาหารและยา. (ม.ป.ป.). คู่มือการขึ้นทะเบียนต ารับ หากไม่มีการแก้ไขและ Bioequivalence
ยาสามัญใหม่, [ออนไลน์]. report ได้รับอนุมัติแล้ว
http://drug.fda.moph.go.th/zone_service/files/drog(d01-05).pdf 04).pdf
5-17 บทที่ 5
สถาบันพระปกเกล้า